- Auteur Jason Gerald gerald@how-what-advice.com.
- Public 2023-12-16 11:11.
- Dernière modifié 2025-01-23 12:18.
La spectrophotométrie est une technique expérimentale utilisée pour mesurer la concentration d'un soluté dans une solution particulière en calculant la quantité de lumière absorbée par cette substance. Cette technique est très utile car certains composés absorberont également différentes longueurs d'onde de lumière à différentes intensités. En analysant la lumière traversant une solution, vous pouvez identifier les composés dissous dans la solution et leurs concentrations. L'outil utilisé pour analyser les solutions avec cette technique en laboratoire est un spectrophotomètre.
Étape
Partie 1 sur 3: Préparation de l'échantillon

Étape 1. Allumez le spectrophotomètre
La plupart des spectrophotomètres doivent être réchauffés avant de pouvoir donner des mesures précises. Alors, démarrez la machine, puis laissez-la reposer pendant au moins 15 minutes avant de mesurer l'échantillon.
Utilisez ce temps pour préparer l'échantillon

Étape 2. Nettoyez la cuvette ou le tube à essai
Dans les laboratoires scolaires, des tubes à essai jetables peuvent être disponibles qui n'ont pas besoin d'être nettoyés au préalable. Cependant, si vous utilisez une cuvette ou un tube à essai ordinaire, assurez-vous de bien nettoyer l'appareil avant utilisation. Rincer toutes les cuvettes avec de l'eau déminéralisée.
- Soyez prudent en utilisant des cuvettes car elles sont assez chères.
- Lors de l'utilisation de la cuvette, ne touchez pas le côté où passe la lumière (généralement le côté transparent du récipient).
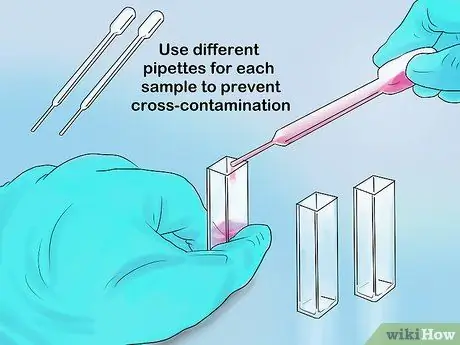
Étape 3. Versez suffisamment d'échantillon dans la cuvette
Le volume maximum d'une partie de la cuvette est de 1 ml, tandis que le volume maximum du tube à essai est de 5 ml. Vos mesures doivent être précises tant que la lumière du spectrophotomètre peut encore traverser l'échantillon et non une partie vide du récipient.
Si vous utilisez une pipette pour insérer des échantillons, utilisez une nouvelle pointe pour chaque échantillon. De cette façon, la contamination croisée peut être évitée

Étape 4. Préparez la solution de contrôle
Ces solutions, également appelées blancs ou blancs, ne contiennent que le solvant de la solution analysée. Par exemple, si vous avez un échantillon de sel dissous dans de l'eau, la solution à blanc dont vous avez besoin est de l'eau. Si l'eau que vous utilisez est rouge, vous devez également utiliser une solution à blanc rouge. Utilisez un récipient similaire pour contenir la solution à blanc dans le même volume que l'échantillon.

Étape 5. Essuyez l'extérieur de la cuvette
Avant d'insérer la cuvette dans le spectrophotomètre, vous devez vous assurer qu'elle est propre pour éviter les interférences avec les mesures dues à des particules de poussière ou des impuretés. Utilisez un chiffon non pelucheux pour éliminer les gouttelettes d'eau ou la poussière adhérant à l'extérieur de la cuvette.
Partie 2 sur 3: Expérimenter

Étape 1. Déterminez et ajustez la longueur d'onde de la lumière pour analyser l'échantillon
Utilisez une seule longueur d'onde de lumière (faisceau monochromatique) pour augmenter l'efficacité de la mesure. Choisissez la couleur de la lumière qui peut être absorbée par le contenu chimique que l'on pense être dissous dans l'échantillon d'essai. Réglez la longueur d'onde en fonction des spécifications du spectrophotomètre que vous utilisez.
- Dans les laboratoires scolaires, ces longueurs d'onde seront généralement données dans les instructions expérimentales.
- Étant donné que l'échantillon reflétera toute la lumière visible, la longueur d'onde de la couleur de la lumière expérimentale est généralement toujours différente de la couleur de l'échantillon.
- Un objet apparaît d'une certaine couleur car il réfléchit une certaine longueur d'onde et absorbe toutes les autres couleurs. L'herbe apparaît verte parce que la chlorophylle qu'elle contient reflète le vert et absorbe d'autres couleurs.
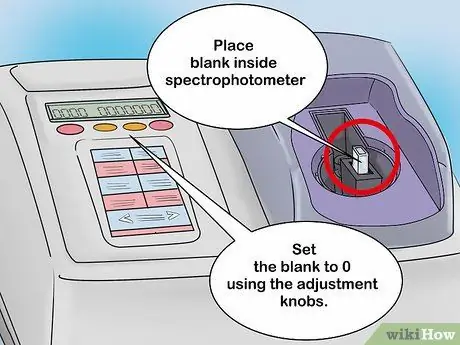
Étape 2. Calibrez le spectrophotomètre avec une solution à blanc
Placer la solution à blanc dans le porte-cuve et fermer le spectrophotomètre. Sur l'écran du spectrophotomètre analogique, il y a une aiguille qui se déplacera en fonction de l'intensité de la détection de la lumière. Une fois la solution à blanc insérée, l'aiguille doit se déplacer vers la droite. Enregistrez cette valeur au cas où vous en auriez besoin plus tard. Laissez la solution à blanc rester dans le spectrophotomètre, puis faites glisser l'aiguille à zéro à l'aide du bouton de réglage.
- Les spectrophotomètres numériques peuvent également être calibrés de la même manière. Cependant, cet outil est équipé d'un écran numérique. Réglez la lecture de la solution à blanc à 0 avec le bouton de commande.
- Même si la solution à blanc est retirée du spectrophotomètre, l'étalonnage sera toujours valide. Ainsi, lorsque vous mesurez l'ensemble de l'échantillon, l'absorbance du blanc sera automatiquement réduite.

Étape 3. Retirez le blanc et testez les résultats de l'étalonnage du spectrophotomètre
Même après avoir retiré la solution à blanc du spectrophotomètre, l'aiguille ou le nombre sur l'écran doit toujours indiquer 0. Remettez la solution à blanc dans le spectrophotomètre et assurez-vous que la lecture ne change pas. Si le spectrophotomètre est correctement calibré à l'aide d'une solution à blanc, le résultat à l'écran doit toujours être 0.
- Si l'aiguille ou le nombre sur l'écran n'indique pas 0, répétez les étapes d'étalonnage avec une solution à blanc.
- Si le problème persiste, demandez de l'aide ou demandez à quelqu'un de vérifier le spectrophotomètre.

Étape 4. Mesurez l'absorbance de l'échantillon
Retirez la solution à blanc et insérez l'échantillon dans le spectrophotomètre. Attendez environ 10 secondes que les aiguilles se stabilisent ou que les chiffres sur l'affichage numérique cessent de changer. Enregistrer le pourcentage de transmission et/ou d'absorbance de l'échantillon.
- Plus il y a de lumière qui passe, moins la lumière est absorbée. Habituellement, vous devez enregistrer la valeur d'absorbance de l'échantillon qui est généralement exprimée sous forme de nombre décimal, par exemple 0,43.
- Répétez la mesure de chaque échantillon au moins trois fois, puis calculez la moyenne. De cette façon, les résultats que vous obtiendrez seront plus précis.

Étape 5. Répétez l'expérience avec différentes longueurs d'onde de lumière
Votre échantillon peut contenir plusieurs composés qui ont des absorbances différentes selon la longueur d'onde de la lumière. Pour réduire l'incertitude, répétez les mesures d'échantillons à des intervalles de longueur d'onde de 25 nm sur tout le spectre lumineux. De cette façon, vous pouvez détecter d'autres produits chimiques dissous dans l'échantillon.
Partie 3 sur 3: Analyse des données d'absorbance

Étape 1. Calculez la transmittance et l'absorbance de l'échantillon
La transmittance est la quantité de lumière qui peut traverser l'échantillon et atteindre le spectrophotomètre. Pendant ce temps, l'absorbance est la quantité de lumière absorbée par l'un des produits chimiques dissous dans l'échantillon. Il existe de nombreux spectrophotomètres modernes donnant une sortie sous forme de transmittance et d'absorbance. Cependant, si vous obtenez une valeur d'intensité lumineuse, vous pouvez également calculer vous-même ces deux valeurs.
- La transmittance (T) peut être déterminée en divisant l'intensité de la lumière traversant la solution échantillon par la quantité de lumière traversant la solution témoin. Cette valeur est généralement exprimée sous forme de nombre décimal ou de pourcentage. T = I/I0, où I est l'intensité de l'échantillon et I0 est l'intensité du blanc.
- L'absorbance (A) est exprimée sous la forme d'un logarithme de base 10 négatif (exposant): A = -log10T. Donc, si T = 0, 1, A = 1 (0, 1 est 10 à la puissance -1). Cela signifie que 10 % de la lumière est transmise, tandis que 90 % est absorbée. Pendant ce temps, si T= 0,01, A = 2 (0,01 est 10 à la puissance -2). Cela signifie que la lumière qui est transmise est de 0,1%.
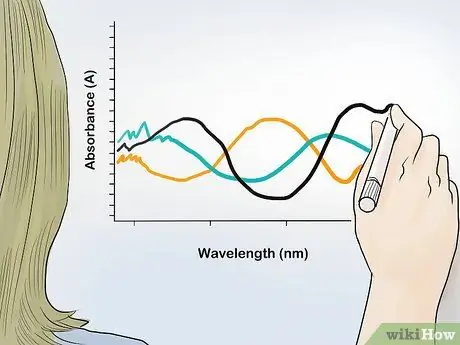
Étape 2. Tracez le graphique de la valeur d'absorbance en fonction de la longueur d'onde
Exprimez la valeur d'absorbance en ordonnée et la longueur d'onde en abscisse. À partir des points de tous les résultats d'absorbance dans chaque longueur d'onde, vous obtiendrez le spectre d'absorbance de l'échantillon et identifierez le contenu du composé et son rapport dans l'échantillon.
Les spectres d'absorbance ont généralement des pics à certaines longueurs d'onde. Ces longueurs d'onde maximales vous permettent d'identifier des composés spécifiques
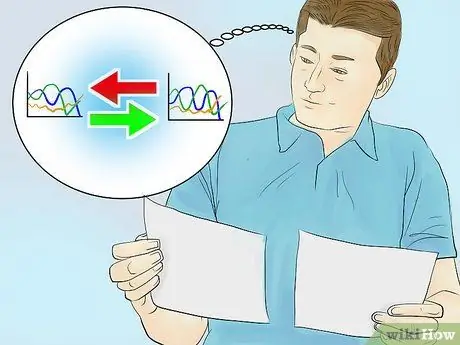
Étape 3. Comparez votre spectre d'absorbance avec un graphique d'un composé connu
Chaque composé a un spectre d'absorbance unique et a toujours la même longueur d'onde de crête dans chaque mesure. En comparant le graphique que vous obtenez avec un graphique d'un certain composé connu, vous pouvez identifier la teneur en soluté dans la solution échantillon.






