- Auteur Jason Gerald gerald@how-what-advice.com.
- Public 2024-01-15 08:14.
- Dernière modifié 2025-01-23 12:18.
Dans une réaction chimique, la matière ne peut être ni créée ni détruite, donc les produits d'une réaction doivent être égaux au nombre de réactifs dans la réaction. La stoechiométrie est l'étude de la relation quantitative des éléments dans une réaction, qui consiste à calculer la masse des réactifs et des produits qu'ils contiennent. La stoechiométrie est une combinaison de mathématiques et de chimie, et est appliquée sur la base d'un principe simple ci-dessus, que la matière n'augmente ou ne diminue jamais dans une réaction. La première étape pour résoudre tout problème de chimie est d'équilibrer les équations.
Étape
Partie 1 sur 4: Équilibrer les équations chimiques

Étape 1. Notez le nombre d'atomes qui composent chaque composé des deux côtés de l'équation
Les équations chimiques peuvent vous aider à identifier les atomes de chaque élément dans une réaction. Dans une réaction chimique, la matière ne peut être ni créée ni détruite, donc une équation est dite inégale si le nombre (et les types) d'atomes constitutifs des deux côtés de l'équation ne sont pas exactement les mêmes.
- N'oubliez pas de multiplier le nombre d'atomes par le coefficient ou le nombre sous la ligne si vous en avez un.
- Par exemple, H2DONC4 + Fe - Fe2(DONC4)3 + H2
- Du côté gauche (réactifs) de l'équation, il y a 2 H, 1 S, 4 O et 1 Fe.
- Du côté droit (produit) de l'équation, il y a 2 H, 3 S, 12 O et 2 Fe.
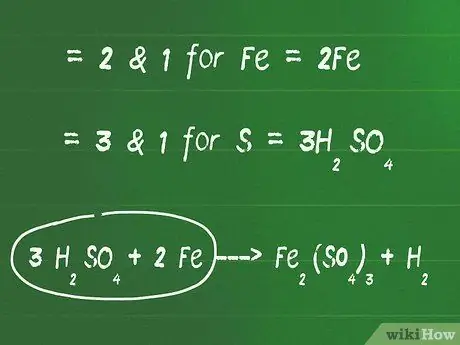
Étape 2. Ajoutez des coefficients devant les éléments autres que l'oxygène et l'hydrogène pour équilibrer les deux côtés de l'équation
Trouvez le plus petit commun multiple d'éléments autres que l'oxygène et l'hydrogène pour égaliser le nombre d'atomes des deux côtés de l'équation.
- Par exemple, le plus petit commun multiple (LCM) entre 2 et 1 est 2 pour Fe. Alors, ajoutez le chiffre 2 devant l'élément Fe sur le côté gauche pour l'équilibrer.
- Le LCM entre 3 et 1 est 3 pour l'élément S. Donc, ajoutez le nombre 3 devant le composé H2DONC4 pour équilibrer les côtés droit et gauche de l'équation.
- A ce stade, l'équation de l'exemple ci-dessus sera: 3 H2DONC4 + 2 Fe - Fe2(DONC4)3 + H2
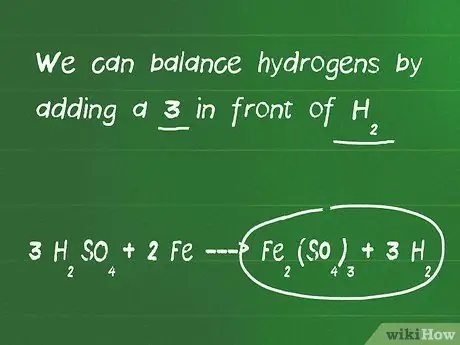
Étape 3. Équilibrez les atomes d'hydrogène et d'oxygène
Le nombre d'atomes d'hydrogène et d'oxygène est équilibré en dernier car ils sont généralement présents dans plusieurs molécules des deux côtés de l'équation. Dans l'étape d'équilibrage de cette équation, n'oubliez pas de recalculer les atomes après avoir ajouté les coefficients devant les molécules.
- Dans l'exemple ici, nous ajoutons le nombre 3 devant le composé H2DONC4, donc maintenant il y a 6 atomes d'hydrogène sur le côté gauche, mais seulement 2 atomes d'hydrogène sur le côté droit de l'équation. Nous avons également actuellement 12 atomes d'oxygène sur le côté gauche et 12 atomes d'oxygène sur le côté droit, donc les atomes d'oxygène sont équivalents.
- On peut équilibrer les atomes d'hydrogène en ajoutant le chiffre 3 devant H2.
- L'équation finale après équilibrage est 3 H2DONC4 + 2 Fe - Fe2(DONC4)3 + 3H2.

Étape 4. Recomptez les atomes des deux côtés de l'équation pour vous assurer qu'ils sont le même nombre
Une fois cela fait, recalculez et vérifiez que l'égalité est la bonne étape. Vous pouvez le faire en additionnant tous les atomes des deux côtés de l'équation et en vous assurant qu'ils sont identiques.
- Vérifiez à nouveau l'égalité de notre équation, 3 H2DONC4 + 2 Fe - Fe2(DONC4)3 + 3H2.
- Sur le côté gauche de la flèche se trouvent 6 H, 3 S, 12 O et 2 Fe.
- Sur le côté droit de la flèche se trouvent 2 Fe, 3 S, 12 O et 6 H.
- Le nombre d'atomes sur les côtés droit et gauche est exactement le même, donc cette équation est déjà équivalente.
Partie 2 sur 4: Conversion de Grammes et Mol
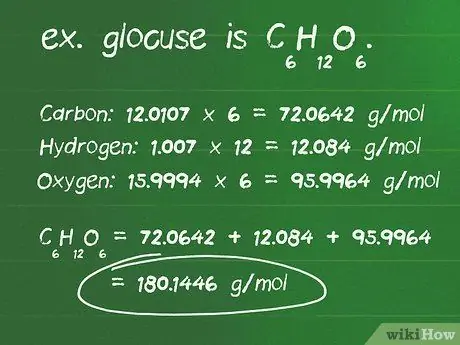
Étape 1. Calculez la masse molaire de la masse du composé donné en grammes
La masse molaire est le nombre de grammes (g) dans une mole d'un composé. Cette unité vous permet de convertir facilement les grammes et les moles d'un composé. Pour calculer la masse molaire, vous devez savoir combien de molécules de l'élément se trouvent dans le composé, ainsi que la masse atomique de chaque élément du composé.
- Trouvez le nombre d'atomes de chaque élément dans un composé. Par exemple, le glucose est C6H12O6, et est composé de 6 atomes de carbone, 12 atomes d'hydrogène et 6 atomes d'oxygène.
- Découvrez la masse atomique en grammes par mole (g/mol) de chaque atome. Les masses atomiques des éléments qui composent le glucose sont: carbone, 12.0107 g/mol; hydrogène, 1,007 g/mole; et oxygène, 15 9994 g/mol.
- Multipliez la masse de chaque atome par le nombre d'atomes présents dans le composé. Carbone: 12,0107 x 6 = 72,0642 g/mol; hydrogène: 1,007 x 12 = 12 084 g/mol; oxygène: 15,9994 x 6 = 95,9964 g/mol.
- La somme de tous les produits ci-dessus est la masse molaire du composé. 72, 0642 + 12, 084 + 95, 9964 = 180, 1446 g/mol. Ou en d'autres termes, la masse d'une molécule de glucose est de 180,14 grammes.
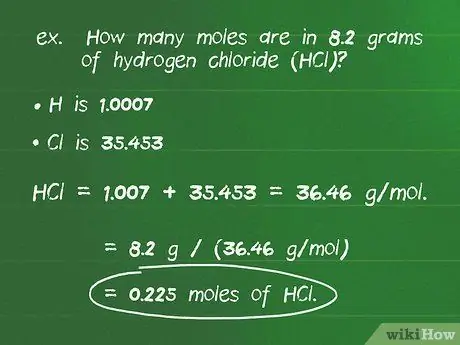
Étape 2. Convertissez la masse d'un composé en moles en utilisant la masse molaire
La masse molaire peut être utilisée comme facteur de conversion, vous pouvez donc calculer le nombre de moles dans un nombre donné de grammes d'échantillon. Divisez la masse connue (g) par la masse molaire (g/mol). Un moyen simple de vérifier vos calculs est de vous assurer que les unités s'annulent et ne laissent que les taupes.
- Par exemple: combien de moles y a-t-il dans 8,2 grammes de chlorure d'hydrogène (HCl) ?
- La masse atomique de H est de 1 0007 et Cl est de 35,453 donc la masse molaire du composé ci-dessus est de 1,007 + 35,453 = 36,46 g/mol.
- En divisant le nombre de grammes du composé par sa masse molaire, on obtient: 8,2 g / (36,46 g/mol) = 0,225 mol HCl.

Étape 3. Déterminez le rapport molaire entre les réactifs
Pour déterminer la quantité de produit produite dans une réaction, vous devez déterminer le rapport molaire. Le rapport molaire est le rapport des composés réagissant les uns avec les autres et est indiqué par les coefficients des composés dans la réaction qui ont été équivalents.
- Par exemple, quel est le rapport molaire de KClO3 avec O2 dans la réaction de 2 KClO3 - 2 KCl + 3 O2.
- Tout d'abord, assurez-vous que les équations ci-dessus sont équivalentes. N'oubliez jamais cette étape ou le rapport molaire obtenu sera faux. Dans cet exemple, les quantités de chaque élément des deux côtés de l'équation sont égales, donc la réaction est équilibrée.
- Le rapport entre KClO3 avec O2 est 2/3. Vous pouvez mettre n'importe quel nombre au-dessus et au-dessous, tant qu'il représente le composé approprié tout au long du problème.

Étape 4. Multipliez la croix par le rapport molaire pour trouver le nombre de moles de l'autre réactif
Pour calculer le nombre de moles d'un composé produit ou requis dans une réaction, vous pouvez utiliser le rapport molaire. Les problèmes de chimie vous demanderont généralement de déterminer le nombre de moles nécessaires ou produites dans une réaction à partir de la masse (grammes) d'un certain réactif.
- Par exemple, dans l'équation de réaction N2 + 3H2 - 2 NH3 combien de moles de NH3 qui résulterait de 3,00 grammes de N2 qui réagit avec H2 en quantité suffisante ?
- Dans cet exemple, H2 disponibles en quantité suffisante et vous n'avez pas à les compter pour résoudre le problème.
- Tout d'abord, changez les unités de grammes N2 être des taupes. La masse atomique de l'azote est de 14,0067 g/mol donc la masse molaire est N2 est de 28,0134 g/mol. La division entre masse et masse molaire donnera 3,00 g/28,0134 g/mol = 0,107 mol.
- Calculer le rapport dans le problème: NH3: N2 = x/0, 107 moles.
- Multipliez ce rapport par le rapport molaire de NH3 avec N2: 2:1 x/0, 107 moles = 2/1 = (2 x 0, 107) = 1x = 0,214 mole.

Étape 5. Convertissez ce nombre de moles en masse en utilisant la masse molaire du composé
Vous utiliserez à nouveau la masse molaire, mais maintenant la masse molaire est nécessaire comme multiplicateur pour renvoyer le nombre de moles en grammes. Assurez-vous d'utiliser la masse molaire correcte du composé.
Masse molaire NH3 est de 17,028 g/mol. Donc 0,214 mole x (17 028 grammes/mol) = 3,647 grammes de NH3.
Partie 3 sur 4: Conversion de litres de gaz et de mole

Étape 1. Découvrez si la réaction a lieu à pression et température standard (STP)
STP est l'ensemble des conditions qui permettent à 1 mole d'un gaz parfait de remplir un volume de 22,414 litres (l). La température standard est de 273, 15 Kelvin (K) et la pression standard est de 1 atmosphère (atm).
Généralement, dans les problèmes, il sera indiqué que la réaction a lieu à 1 atm et 273 K, ou en STP
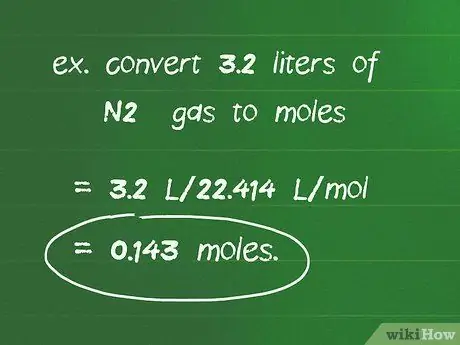
Étape 2. Utilisez le facteur de conversion de 22 414 l/mol pour convertir le nombre de litres de gaz en moles de gaz
Si la réaction a lieu dans des conditions STP, vous pouvez utiliser 22,414 l/mol pour calculer le nombre de moles dans un volume de gaz connu. Divisez le volume de gaz (l) par ce facteur de conversion pour trouver le nombre de moles.
Par exemple, pour convertir 3,2 litres de N2 gaz en moles: 3,2 l/22, 414 l/mol = 0,143 mol.

Étape 3. Utilisez la loi des gaz parfaits pour convertir des litres de gaz si ce n'est pas dans des conditions STP
Si la réaction dans le problème n'a pas lieu dans des conditions STP, vous devez utiliser la loi des gaz parfaits PV = nRT pour calculer le nombre de moles dans une réaction. P est la pression en unités atmosphériques, V est le volume en litres, n est le nombre de moles, R est la constante de la loi des gaz, 0,0821 l-atm/mol-degrés et T est la température en degrés Kelvin.
- Cette équation peut être réarrangée pour calculer les moles, pour devenir: n = RT/PV.
- Les unités de la constante de gaz sont conçues pour éliminer toutes les autres variables unitaires.
- Par exemple, déterminez le nombre de moles dans 2,4 litres d'O2 à 300 K et 1,5 atm. En branchant les variables dans l'équation, on obtient: n = (0,0821 x 300)/(1, 5 x 2) = 24, 63/3, 6 = 6, 842 moles O2.
Partie 4 sur 4: Conversion de litres de liquides et de Mol
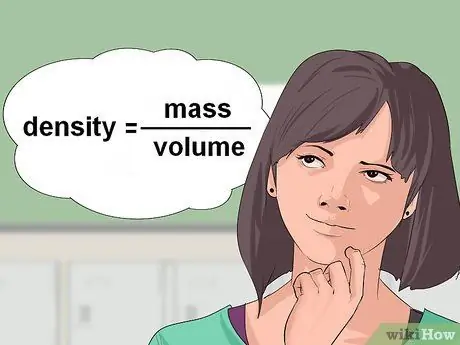
Étape 1. Calculez la densité du liquide
Parfois, des équations chimiques vous donnent le volume de réactif liquide et vous demandent de calculer le nombre de grammes ou de moles nécessaires à la réaction. Pour convertir le volume d'un liquide en grammes, vous avez besoin de la densité du liquide. La densité est exprimée en unités de masse/volume.
Si la densité est inconnue dans le problème, vous devrez peut-être la rechercher dans un manuel ou sur Internet

Étape 2. Convertissez le volume en millilitres (ml)
Pour convertir le volume d'un liquide en masse (g), vous devez utiliser sa densité. La densité est exprimée en grammes par millilitre (g/ml), donc le volume d'un liquide doit également être exprimé en millilitres pour le calculer.
Découvrez le volume connu. Par exemple, disons dans le problème que le volume de H. est connu2O est 1 litre. Pour le convertir en ml, il suffit de le multiplier par 1000 car il y a 1000 ml dans 1 litre d'eau.

Étape 3. Multipliez le volume par la densité
En multipliant le volume (ml) par sa densité (g/ml), les unités ml sont perdues et ce qui reste est le nombre de grammes du composé.
Par exemple, la densité H2O est de 18,0134 g/ml. Si l'équation chimique dit qu'il y a 500 ml de H2O, le nombre de grammes dans le composé est de 500 ml x 18,0134 g/ml ou 9006, 7 g.
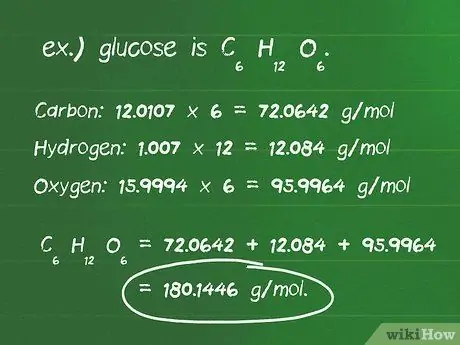
Étape 4. Calculez la masse molaire des réactifs
La masse molaire est le nombre de grammes (g) dans une mole d'un composé. Cette unité vous permet de changer les unités de grammes et de moles dans un composé. Pour calculer la masse molaire, vous devez déterminer combien de molécules de l'élément se trouvent dans un composé, ainsi que la masse atomique de chaque élément du composé.
- Déterminer le nombre d'atomes de chaque élément dans un composé. Par exemple, le glucose est C6H12O6, et est composé de 6 atomes de carbone, 12 atomes d'hydrogène et 6 atomes d'oxygène.
- Découvrez la masse atomique en grammes par mole (g/mol) de chaque atome. Les masses atomiques des éléments du glucose sont: carbone, 12,0107 g/mol; hydrogène, 1,007 g/mole; et oxygène, 15 9994 g/mol.
- Multipliez la masse atomique de chaque élément par le nombre d'atomes présents dans le composé. Carbone: 12,0107 x 6 = 72,0642 g/mol; hydrogène: 1,007 x 12 = 12 084 g/mol; oxygène: 15,9994 x 6 = 95,9964 g/mol.
- Additionnez les résultats de la multiplication ci-dessus pour obtenir la masse molaire du composé, qui est 72, 0642 + 12, 084 + 95, 9964 = 180, 1446 g/mol. Ainsi, la masse d'une mole de glucose est de 180,14 grammes.

Étape 5. Convertissez le nombre de grammes d'un composé en moles en utilisant la masse molaire
En utilisant la masse molaire comme facteur de conversion, vous pouvez calculer le nombre de moles présentes dans un nombre donné de grammes d'échantillon. Divisez le nombre de grammes (g) du composé connu par la masse molaire (g/mol). Un moyen simple de vérifier vos calculs est de vous assurer que les unités s'annulent et ne laissent que les taupes.
- Par exemple: combien de moles y a-t-il dans 8,2 grammes de chlorure d'hydrogène (HCl) ?
- La masse atomique de H est de 1 0007 et Cl est de 35,453 donc la masse molaire du composé est de 1,007 + 35,453 = 36,46 g/mol.
- En divisant le nombre de grammes du composé par la masse molaire, on obtient: 8,2 g/(36,46 g/mol) = 0,225 mol HCl.






